| |
 |
|
| ▲ 한미약품 본사 전경./사진=한미약품 |
[미디어펜=김견희 기자]한미약품이 얀센서 기술반환된 당뇨·비만 신약 후보물질 LAPS GLP·Glucagon 수용체 듀얼 아고니스트(HM12525A)를 비알코올성 지방간염(NASH) 치료제로 MSD에 기술수출하는 쾌거를 이루면서 연구개발 중인 파이프라인에 대한 관심도 높아지고 있다.
5일 업계에 따르면 故임성기 한미약품 회장은 R&D에 대한 뚝심 하나로 한미의 앞날을 밝힐 여러 파이프라인을 남겼다. 한미약품이 현재 보유하고 개발 중인 파이프라인은 총 26개로 바이오 신약 14개, 합성 신약 12개로 나뉜다.
주요 파이프라인은 한미약품의 독자적인 랩스커버리 기술이 적용된 당뇨병 치료제 에페글레나타이드를 비롯해 성장호르몬 결핍증 치료제 '에페소마트로핀'과 NASH(비알코올성지방간염) 치료제 'HM15211', 호중구 감소증 치료제 '롤론티스' 등이 있다.
합성신약은 포지오티닙과 항암제로 개발 중인 '오락솔'과 '오라테'칸, '오라독셀', '벨바라페닙' 등 항암제가 주를 이루고 있으며 자가면역질환 치료제 'HM71224'와 미국 알레그로에 투자해 독점권을 확보한 '루미네이트' 등이 꼽힌다.
파이프라인들 중 가장 개발 속도가 진척된 약물은 롤론티스다. 2012년 스펙트럼에 기술수출한 롤론티스는 현재 글로벌 임상3상까지 마쳤으며 올해 10월 미국 식품의약국(FDA)의 판매허가 여부를 앞두고 있다. 회사 관계자는 "10월 말 검토가 끝나고 하반기 허가 예정으로 내다보고 있다"고 말했다.
2011년 아테넥스에 항암 신약 후보물질로 기술수출한 오락솔도 현재 임상3상 단계로 FDA 신약 허가 신청을 앞두고 있다. 오락솔에는 주사용 항암제를 경구용으로 바꾸는 한미약품의 플랫폼 기술 '오라스커버리'가 적용됐다.
| |
 |
|
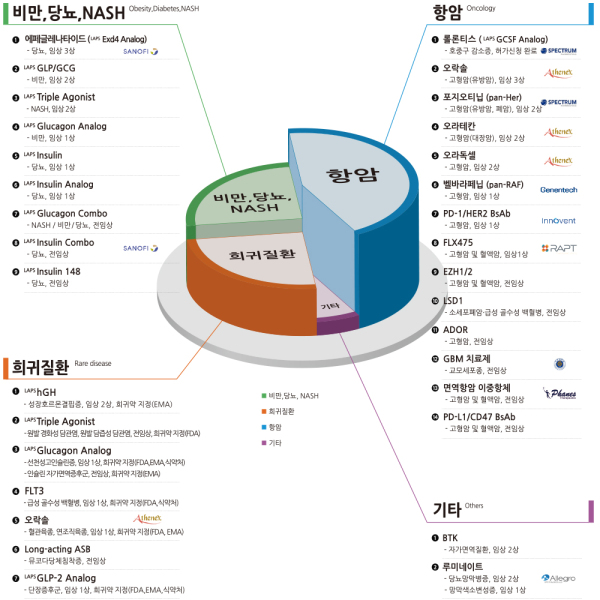
| ▲ 한미약품이 개발 중인 파이프라인./사진=한미약품 |
포지오티닙도 업계를 중심으로 긍정적인 평가를 받고 있다. 두 번째 코호트 시험 결과가 연구진의 예상치 보다 우수하게 나왔기 때문. 회사 관계자는 "두 번째 코호트 시험 결과가 예상치보다 좋게 나와서 신약허가신청(NDA)에 긍정적으로 작용할 수 있을것으로 내다보고 있다"고 말했다.
개발 파트너사 스펙트럼은 지난달 글로벌 임상 2상의 두 번째 코호트 연구결과를 발표하면서 FDA 허가신청을 위한 미팅을 추진한다고 밝힌 바 있다. 만약 포지오티닙이 FDA의 허가를 받게 된다면 한미약품이 지난 2015년 기술수출했던 파이프라인 5개 중 처음으로 상업화에 성공하게 되는 것이다.
이번에 MSD로 기술수출한 HM12525A도 주목된다. 한미약품의 LAPS GLP/Glucagon 수용체 듀얼 아고니스트는 지난 2015년 얀센에 HM12525A라는 코드명으로 기술이전된 바 있다. 하지만 얀센은 지난해 체중 감소 목표치는 도달했으나 당뇨를 동반한 비만 환자의 혈당 조절이 내부 기준치에 미치지 못하자 권리를 반환했다.
HM12525A은 실패로 돌아가는 듯했으나 한미약품은 이에 포기하지 않고 새로운 적응증을 탐색한 결과 1년 여만에 NASH 치료제로 개발, 제조하는 1조원 규모의 라이선스 계약을 MSD와 체결했다. 다소 시행착오를 겪었지만 기술반환된 약물에서 새로운 적응증을 찾아내는 성과를 맺은 셈이다.
이같은 결실은 1973년 창업 이후 지난 48년 간 일궈온 임 회장의 신약 연구개발에 대한 의지와 투자의 결과라는 평가를 받는다. 임 회장은 살아 생전 "R&D 없는 제약은 죽은 산업"이라는 신념으로 시종일관 연구개발의 필요성을 강조했다.
[미디어펜=김견희 기자]
▶다른기사보기